毒劇ドットコム
毒物劇物取扱者.com
複数条件の場合はキーワードの間にスペースを入れてください。例 特定毒物 劇物
気体の性質(7問)
毒物劇物取扱者試験は、基本的問題のみが出題されまのでサクサク解ける問題が多いです。
あまり凝った問題は出ませんので確実に得点していくことを願っています。
問題01
ある気体を容器に入れ、$8.3 \times 10^{5}[Pa]$、$127[ ^\circ C ]$に保ったとき、気体の密度は$4.0[g/L]$であった。この気体の分子量として適切なものは次のうちどれか。
ただし、この気体は理想気体とする。また、気体定数は、$8.3 \times 10^{3}[Pa \cdot L/(K \cdot mol)]$とし、絶対温度$T[K]$とセ氏温度(セルシウス温度)$t[^\circ C]$の関係は、
$T=t+273$とする。
東京都 2020年
解 説
理想気体の状態方程式
\[ \begin{align*} P \cdot V =\underbrace{ \frac{w}{M}}_{物質量[mol]} \cdot R \cdot T \ \ \ \cdots ① \end{align*} \]
より、
\[ \begin{align*} 8.3 \times 10^{5} \times V = \frac{w}{M} \times 8.3 \times 10^{3} \times(273+127) \ \ \ \cdots ② \end{align*} \]
この問題の重要ポイントになります。
このときの気体の密度は$4.0[g/L]$であることから、
\[ \begin{align*} \frac{w[g]}{V[L]} = 4.0[g/L] \ \ \ \ \ \ \cdots ③ \end{align*} \]
②式、③式より
\[ \begin{align*} 8.3 & \times 10^{5} \times M = \frac{w}{V} \times 8.3 \times 10^{3} \times400 \\ M &= \frac{4 \times 400}{100} \\ &=16 \end{align*} \]
問題02
体積$3.0[L]$の容器に、ある気体$0.50[mol]$を入れて$27[ ^\circ C ]$に保ったとき、気体の圧力$[Pa]$ として 適切なものはどれか。 なお、気体定数は、$8.3 \times 10^{3}[Pa \cdot L/(K \cdot mol)]$とし、絶対温度$T[K]$とセ氏温度(セルシウス温度)$t[^\circ C]$の関係は、$T=t+273$とする。
東京都 2018年
解 説
気体の状態方程式$PV=nRT$より、
$P \times 3.0 = 0.5 \times 8.3 \times 10^{3} \times(273+27)$
$P=4.15 \times 10^{3} [Pa]$
問題03
体積$8.3[L]$の容器に、ある気体$0.50[mol]$を入れて$27[ ^\circ C ]$に保ったとき、気体の圧力$[Pa]$ として 適切なものはどれか。 なお、気体定数は、$8.3 \times 10^{3}[Pa \cdot L/(K \cdot mol)]$とし、絶対温度$T[K]$とセ氏温度(セルシウス温度)$t[^\circ C]$の関係は、$T=t+273$とする。
東京都2016年
解説
気体の状態方程式$PV=nRT$より、
$P \times 8.3 = 0.5 \times 8.3 \times 10^{3} \times(273+27)$
$P=1.5 \times 10^{5} [Pa]$
問題04
標準状態($0[^\circ C]$、$1.013 \times 10^{5}[Pa]$)において、二酸化炭素$2.24[L]$中の酸素原子の物質量として、適切なものは次のうちどれか。 ただし、標準状態における$1[mol]$の気体の体積は$22.4[L]$とする。
茨城県
解 説
\[ \begin{align*} 物質量[mol] &=\frac{気体の体積(標準状態)[L]}{22.4[L/mol]} \\ \\ &=\frac{2.24[L]} {22.4[L]/mol} \\ \\ &=0.10[mol] \end{align*} \]
二酸化炭素の化学式は$\ce{CO2}$であり、$0.1[mol]$中に含まれる$\ce{CO2}$の酸素原子$\ce{O}$は、
\[ \begin{align*} 0.10 \times 2 = 0.20[mol] \end{align*} \]
となります。
問題05
$27[ ^\circ C ]$、$6.0 \times 10^{4}[Pa]$で$0.20[mol]$の気体の体積として 適切なものはどれか。 なお、気体定数は、$8.3 \times 10^{3}[Pa \cdot L/(K \cdot mol)]$とし、絶対温度$T[K]$とセ氏温度(セルシウス温度)$t[^\circ C]$の関係は、$T=t+273$とする。
千葉県
解 説
理想気体の状態方程式
\[ \begin{align*} &PV=nRT \\ &6.0 \times 10^{4} \times V = 0.20 \times 8.3 \times 10^{3} \times(273+127) \\ V&= \frac{0.20 \times 8.3 \times 10^{3} \times300}{6.0 \times 10^{4} } \\ &= 8.3[L] \end{align*} \]
問題06
容積$10[L]$の容器の内部を真空にして、水$5.4[g]$を注入後、容器内の温度を$60[ ^\circ C ]$に保ったとき、容器の中に液体として存在する水の質量として、最も近いものは次のうちどれか。 ただし、原子量は$\ce{H=1}$、$\ce{O=16}$、気体定数は、$8.3 \times 10^{3}[Pa \cdot L/(K \cdot mol)]$とし、絶対温度$T[K]$とセ氏温度(セルシウス温度)$t[^\circ C]$の関係は、$T=t+273$とする。
東京都2021年
解 説
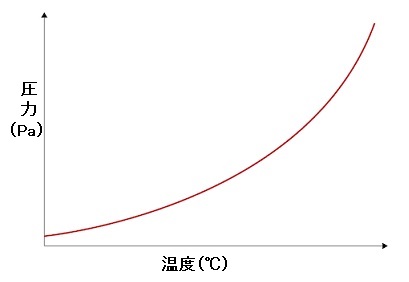
体積一定で温度を上げていくと、気体は徐々に蒸発し、気相中に存在する気体のmol数が増えます。
これに伴い圧力(飽和蒸気圧)が増加します。
このような圧力(飽和蒸気圧)と温度の関係を表す曲線を蒸気圧曲線といい、状態図の一部を切り取ったものです。
$60[ ^\circ C ]$における気体の状態方程式から水の質量$w[g]$を求めます。
\[ \begin{align*} &P \cdot V = \underbrace{\frac{w}{M}}_{物質量[mol]} \cdot R \cdot T \\ &w:質量[g] \\ &M:分子量 \\ &2.0\times10^{4}[Pa]\times10[L]=\frac{w[g]}{18}\times8.3 \times 10^{3}\times(273+60[ ^\circ C ])\\ \\ w&=\frac{2.0\times10^{4}\times10}{8.3 \times 10^{3}\times333}\\ &=\frac{200\times18}{8.3\times333}\\ &\fallingdotseq 1.3[g]\\ \end{align*} \]
これが水蒸気の質量です。
液体として存在する水の質量は、注入した水が$5.4[g]$でそのうち$1.3[g]$が水蒸気ですから
$5.4-1.3=4.1[g]$となります。
問題07
容器の内部を真空にして、水$0.010[mol]$を注入後、容器内の水をすべて蒸発させる容器の体積として、最も近いものは次のうちどれか。 ただし、容器内の温度を$27[ ^\circ C ]$に保ち、$27[ ^\circ C ]$の水の飽和蒸気圧を$8.3 \times 10^{3}[Pa]$ 、気体定数は、$8.3 \times 10^{3}[Pa \cdot L/(K \cdot mol)]$とし、絶対温度$T[K]$とセ氏温度(セルシウス温度)$t[^\circ C]$の関係は、$T=t+273$とする。
オリジナル問題
解 説
$0.010[mol]$の水がちょうど蒸発したとき、水蒸気の圧力は$3.0 \times 10^{3}[Pa]$です。
そのときの容器の体積$V[L]$は、気体の状態方程式$PV=nRT$から求められます。
$3.0 \times 10^{3} \times V= 0.010 \times 8.3 \times 10^{3} \times(273+27)$
∴$V=8.3[L]$
以上
Dokugeki.com hopes you will successfully complete poisonous and deleterious substance handler test.
I would be delighted if this website is helpful for you to obtain the license.
Fortune prefers a person who has prepared minds.
Copyright (C) Since 2015 毒物劇物取扱者.com All Rights Reserved.