毒劇ドットコム
毒物劇物取扱者.com
複数条件の場合はキーワードの間にスペースを入れてください。例 特定毒物 劇物
二クロム酸カリウム
酸化剤
二クロム酸カリウム$\ce{K2Cr2O7}$は赤橙色の結晶で水に溶けると電離してニクロム酸イオン$ \mathrm{ Cr_{2}O_{7} \hspace{1pt} ^{2-} }$を生じます。
このイオンの$\ce{Cr}$の酸化数は+6で周期表6族の$\ce{Cr}$にとって最高酸化数にあたります。
酸性溶液中($\ce{H+}$が浮遊)では他の物質から電子を奪って(還元)、酸化数が+3のクロム(Ⅲ)イオン$\ce{Cr^{3+}}$(暗緑色)になる傾向を持ち強い酸化作用を示します。
酸化剤は相手を酸化し自分は還元される(電子を受け取る)物質、還元剤は相手を還元し自分自身は酸化される(電子を失う)物質のことです。
酸化剤と還元剤を混合すると、電子の授受に基づく酸化還元反応が起こります。
酸化剤$\ce{K2Cr2O7}$の半反応式の作り方をついて述べます。
酸化剤とその生成物の化合式を書きます。
$ \mathrm{ Cr_{2}O_{7} \hspace{1pt} ^{2-} } \ce{ -> Cr^{3+} } $
酸素原子の酸化数は-2、生成物のクロム(Ⅲ)イオンの酸化数は+3です。
$\begin{align*} \mathrm{ \underset{?}{\underline{Cr}} \hspace{1pt} _{2} \underset{-2}{\underline{O}} \hspace{1pt} _{7} \hspace{1pt} ^{2-} \longrightarrow \underset{+3}{\underline{Cr}} \hspace{1pt} ^{3+} } \end{align*} $
$ \mathrm{ Cr_{2}O_{7} \hspace{1pt} ^{2-} } $の中の$\ce{Cr}$の酸化数$x$を求めます。
$x \times 2 + (-2) \times 7 = -2 $
$x = +6$
となります。
$\begin{align*} \mathrm{ \underset{+6}{\underline{Cr}} \hspace{1pt} _{2} \underset{-2}{\underline{O}} \hspace{1pt} _{7} \hspace{1pt} ^{2-} \longrightarrow \underset{+3}{\underline{Cr}} \hspace{1pt} ^{3+} } \end{align*} $
生成物の$\ce{Cr}$の酸化数は+3となり、酸化数が減少していますので還元されていることが分かります。
酸化数変化があるのはクロム$\ce{Cr}$です。
両辺の酸化数変化がある原子、この例題ではクロム$\ce{Cr}$の数を調整します。
$\begin{align*} \mathrm{ \underset{+6}{\underline{Cr}} \hspace{1pt} _{2} \underset{-2}{\underline{O}} \hspace{1pt} _{7} \hspace{1pt} ^{2-} \longrightarrow 2 \underset{+3}{\underline{Cr}} \hspace{1pt} ^{3+} } \end{align*} $
両辺の酸化数の変化を$\ce{e-}$で調整します。
$\ce{Cr}$1個の酸化数が左辺では+6、右辺では+3ですから、3個の電子を受け取っている(還元)と思いがちですが、左辺は$\ce{Cr2}$、左辺は$\ce{2Cr}$のため2倍の+6の電子を左辺に足して調整します。
$\begin{align*} \mathrm{ \underset{+6}{\underline{Cr}} \hspace{1pt} _{2} \underset{-2}{\underline{O}} \hspace{1pt} _{7} \hspace{1pt} ^{2-} +\underbrace { 6e^-}_{得た電子} \longrightarrow 2 \underset{+3}{\underline{Cr}} \hspace{1pt} ^{3+} } \end{align*} $
両辺の電荷(イオンの価数)を$\ce{H+}$で調整します。
$\begin{align*} \mathrm{ \underbrace{ Cr_{2}O_{7} \hspace{1pt} ^{2-} + 6e^- }_{(2-)+(6-)} \longrightarrow \underset{6+}{\underline{2Cr}} \hspace{1pt} ^{3+} } \end{align*} $
電荷が8-が6+になっていますので、左右辺どちらに$\ce{H+}$何個足せばよいでしょうか。
左右の電荷数が等しくなるためには、左辺に14+が必要ですから$\ce{H+}$を左辺に加えます。
$\begin{align*} \mathrm{ \underbrace{ Cr_{2}O_{7} \hspace{1pt} ^{2-} + 6e^- }_{(8-)} + \underbrace{14 H^+ }_{14+} \longrightarrow \underset{6+}{\underline{2Cr}} \hspace{1pt} ^{3+} } \end{align*} $
両辺の$\ce{H}$と$\ce{O}$の原子数を$\ce{H2O}$で調整します。
$\ce{14H+}$ですからの7個の$\ce{H2O}$を右辺に加えます。
$ \mathrm{ Cr_{2}O_{7} \hspace{1pt} ^{2-} + 6e^- + 14H^+ } \ce{ -> 2Cr^{3+} + 7H2O } $
問題
原子の酸化数として、適切なものは、次のうちどれか。
埼玉県
解 説
(1)$\ce{H2O2}$の$\ce{O}$の酸化数は-1である。
選択肢(1)が適切です。
例外的に過酸化水素$\ce{H2O2}$は、$\ce{O}$の酸化数を-1とします。
一般的には化合物中の水素原子の酸化数は+1、酸素原子の酸化数は-2としています。
化合物中の原子の酸化数の総和は、0です。
$\begin{align*} \mathrm{ \underset{+1}{\underline{H}} \hspace{1pt} _{2} \underset{-1}{\underline{O}} \hspace{1pt} _{2} } \end{align*} $
$\ce{H2O2}$‥‥(+1)×2+(-1)×2=0
(2)$\ce{FeCl3}$の$\ce{Fe}$の酸化数は-3である。
選択肢(2)は不適切です。
$\begin{align*} \mathrm{ \underset{x}{\underline{Fe}} \hspace{2pt} \underset{-1}{\underline{Cl}} \hspace{1pt} _{3} } \end{align*} $
$\ce{FeCl3}$‥‥$x$+(-1)×3=0
$x = +3$
$\ce{Fe}$の酸化数は+3となります。
(3)$\ce{NH4 } \hspace{1pt} ^{+}$の$\ce{N}$の酸化数は-4である。
選択肢(3)も不適切です。
多原子イオン中の原子の酸化数の総和は、そのイオンの電荷です。
$\begin{align*} \mathrm{ \underset{x}{\underline{N}} \hspace{2pt} \underset{+1}{\underline{H}} \hspace{1pt} _{4} \hspace{1pt} ^+ } \end{align*} $
$\ce{NH4 } \hspace{1pt} ^{+}$‥‥$x$+(+1)×4=+1$x$=1-4=-3
$\ce{N}$の酸化数は-3となります。
$\ce{K2Cr2O7}$の酸化数を$x$とおきます。
$\begin{align*} \mathrm{ \underset{+1}{\underline{K}} \hspace{1pt} _2 \hspace{2pt} \underset{x}{\underline{Cr}} \hspace{1pt} _2 \underset{-2}{\underline{O}} \hspace{1pt} _{7} } \end{align*} $
$\ce{K2Cr2O7}$‥‥(+1)×2+$x$×2 +(-2)×7=0
$2x$=-2+14
$x$=+6
別解
$\ce{K2Cr2O7 -> 2K+ + Cr2O7 } \hspace{1pt} ^{2-} $
$ \mathrm{ Cr_{2}O_{7} \hspace{1pt} ^{2-} } $の中の$\ce{Cr}$の酸化数$x$を求めます。
$x \times 2 + (-2) \times 7 = -2 $
$x = +6$
$\ce{Cr}$の酸化数は+6となります。
- $\ce{H}$は+1、$\ce{O}$は-2
- アルカリ金属は+1、アルカリ土類金属は+2、ハロゲンは-1
- 単体中の原子は0、イオンは価数
- 分子内の総和は0
イオン内の総和は価数
$\ce{Cr^3+}$について
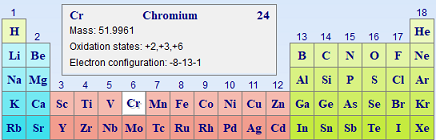
クロムは原子番号24です。
電子は24個です。
4f
4d
4p
4s 1個 N殻
3s 2個 3p 6個 3d 5個 M殻
2s 2個 2p 6個 L殻
1s 2個 K殻
3d軌道の最大収容電子数が10であり、d軌道の収容電子数が5個と10個になったとき特別に元素の安定性が増します。
$\ce{Cr^3+}$は、4s軌道の電子一つと3d軌道の電子二つが取り除かれた(奪われた)ものです。
4f
4d
4p
4s 0個 N殻
3s 2個 3p 6個 3d 3個 M殻
2s 2個 2p 6個 L殻
1s 2個 K殻
元々の3d軌道の5つの軌道のうち、3つは3p軌道とわりと近く、エネルギー的にも低い軌道なため$\ce{Cr^3+}$は安定です(そういう状態になりたがる)。
Dokugeki.com hopes you will successfully complete poisonous and deleterious substance handler test.
I would be delighted if this website is helpful for you to obtain the license.
Fortune prefers a person who has prepared minds.
Copyright (C) Since 2015 毒物劇物取扱者.com All Rights Reserved.